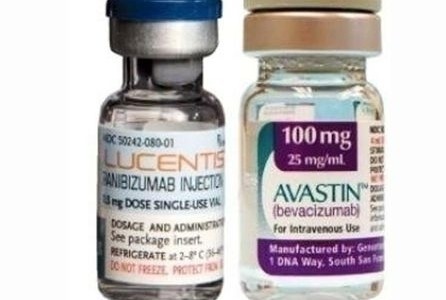
La Guardia di finanza ha perquisito gli uffici dell’Aifa l’Agenzia Italiana del Farmaco, ed ha acquisito documenti e delibere inerenti la vicenda Avastin-Lucentis, i due farmaci oftalmici al centro di un caso di arbitrario innalzamento del prezzo da parte di due grandi multinazionali farmaceutiche come Roche e Novartis.
La perquisizione e l’acquisizione dei documenti e’ stata eseguita su mandato della Procura di Roma. Nell’inchiesta del pm Stefano Pesci e dell’aggiunto Nello Rossi risultano almomento indagate i vertici delle societa’ farmaceutiche Roche e Novartis. Le accuse ipotizzate dagli inquirenti sono: aggiotaggio, truffa aggravata ai danni dello Stato e disastro doloso. Secondo quanto si e’ appreso gli inquirenti hanno come obiettivo quello di ricostruire le trattative per la definizione del prezzo di Avastin e Lucentis dal 2009 ad oggi.
Nel fattempo il Ministero della Salute fa sapere che ”ha provveduto gia’ da diversi giorni ad inoltrare alla Roche Spa, alla Novartis Farma Spa e alla Pfizer Italia Srl specifici atti di diffida e messa in mora, con efficacia anche di atti interruttivi della prescrizione, con richiesta di risarcimento dei danni patrimoniali e non patrimoniali arrecati al Servizio sanitario nazionale”. La precisazione del Ministero e’ arrivata ieri in serata, in risposta a quanto diffuso da alcuni organi di informazione che denunciavano una mancata richiesta di risarcimento del Ministero nei confronti della Societa’ Roche S.pA relativamente al caso Avastin-Lucentis.
Occorre ricordare che l’Aifa si era espressa contro lo stesso ministero della Salute affermando che il farmaco più economico era stato riconosciuto come “dannoso”, dunque sposando le operazioni delle due multinazionali che avevano ritirato uno dei prodotti gemelli (quello più economico) per lasciare tutto il mercato (e dunque anche gli acquisti da parte del sistema sanitario) a quello più costoso. Emblematico di questa intesa tra agenzia del farmaco, multinazionali e istituzioni era la nota diffuso a marzo dalla direzione generale della Salute della Commissione europea, la quale ha ritenuto che “l’Aifa abbia agito nel rispetto delle regole e nell’interesse dei pazienti”. Lo aveva affermato Paola Testori Coggi, Direttore Generale della Direzione Generale della Salute e dei Consumatori della Commissione Europea. Una intesa rivelatrice dei mandanti e della natura di molte direttive europee.
Ma a metà maggio, contro la decisione delle due multinazionali e dell’Aifa di ritirare il farmaco più economico, su richiesta del ministero della Salute si era espresso anche il Consiglio Superiore di Sanità: “I due farmaci – si legge nel parere del Css- non presentano differenze statisticamente significative dal punto di vista dell’efficacia e della sicurezza nella terapia della degenerazione maculare senile”, anche se le molecole sono differenti. Il Css ritiene dunque possibile l’utilizzo il “più presto possibile dell’Avastin per il trattamento della degenerazione maculare senile”, con un dosaggio che consenta la somministrazione adeguata del farmaco oggi resa difficile dal fatto che non viene confezionato in singole dosi ma in un unico flacone”. Anche ad occhio emerge che c’è parecchio da scavare dentro l’Aifa ma anche nelle relazioni particolari tra multinazionali e Commissione Europea.
- © Riproduzione possibile DIETRO ESPLICITO CONSENSO della REDAZIONE di CONTROPIANO
Ultima modifica: stampa